
コーヒー中に含まれる代表的なポリフェノールとして、クロロゲン酸類が広く知られている。クロロゲン酸類は、一般に桂皮酸誘導体とキナ酸のエステル化合物と定義される。コーヒー中には主にカフェオイルキナ酸、フェルロイルキナ酸、ジカフェオイルキナ酸からなる9種類の化合物が含まれており、これらの総称をクロロゲン酸類とする。本品には関与成分としてカフェオイルキナ酸、フェルロイルキナ酸の主要6成分のクロロゲン酸類を270 mg含有し、ヒドロキシヒドロキノンを低減したコーヒー飲料である。
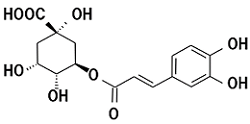
【関与成分の構造式】
クロロゲン酸類の代表的化合物名:
5-カフェオイルキナ酸 (5-CQA)
 |
本品の関与成分であるクロロゲン酸類には以下の作用・効果および機序が確認されている。 1) 動物試験による継続摂取試験において、体重増加抑制、内臓脂肪重量の低下が認められ、その関与成分はクロロゲン酸類であると確認した。作用機序としてクロロゲン酸類の継続摂取によりエネルギー消費量が高くなり、脂質燃焼量が増加していることを確認した (PMID:20943752) 。 2) 有効性および作用機序をヒトで検証したところ、12週間継続摂取によりヒトの腹部脂肪面積、体重、BMI、ウエスト周囲長、およびヒップ周囲長の減少が認められ (2009211385) 、ヒトのエネルギー消費量、脂肪燃焼量の増加が確認された (2011149729) 。
(PMID20943752) Am J Physiol Endocrinol Metab. 2011:300(1);E122-133. (2009211385) 薬理と治療. 2009:37(4);333-344. (2011149729) J Health Sci. 2010:56(6);745-751.
関与成分 (クロロゲン酸類) は、クロロゲン酸類主要6成分 [3-カフェオイルキナ酸 (3-CQA) 、4-カフェオイルキナ酸 (4-CQA) 、5-カフェオイルキナ酸 (5-CQA) 、3-フェルロイルキナ酸 (3-FQA) 、4-フェルロイルキナ酸 (4-FQA) 、5-フェルロイルキナ酸 (5-FQA)] の総量とし、高速液体クロマトグラフィーにより分析した (1) 。
(1) 社内報告書
研究1: 過剰摂取試験 対象BMI 30.0 kg/m2未満の成人男女35名。 方法:市販品相当のコーヒーを対照飲料とした4週間継続摂取による無作為化割付二重盲検並行群間試験を実施した。試験は事前観察期間を約3週間、試験飲料摂取期間を4週間、事後観察期間を2週間設けた。事前観察期間中の検査後、被験者を2群 (クロロゲン酸飲料群:Active群と対照飲料群:Control群) に分けた。クロロゲン酸飲料は1本あたりクロロゲン酸類を297 mg含むコーヒー飲料とした。試験飲料摂取期間中、被験者はクロロゲン酸飲料 (内容量:185 g/本) もしくは対照飲料 (内容量:185 g/本) を1日3本4週間摂取した。検査項目は、自覚症状、血液・尿検査、および理学的検査とした。試験期間中、被験者には他のコーヒー飲料の摂取を禁止すると共に、生活習慣や運動習慣を変えないよう指導した。 結果:試験飲料摂取により、理学的検査項目や血液・尿検査項目に問題となる変動は認められなかった。被験者の自覚症状の記録より、消化器系、もしくは腎・泌尿器系に関する症状を訴えたActive群の4名とControl群の1名について、試験責任医師は試験飲料との因果関係を否定できないため、これら症状を副作用と判定した。しかし、それらは軽微で一過的であり、一般的なコーヒーを摂取したときにも認められる症状であったため、最終的に試験責任医師は、Active飲料の過剰摂取はControl飲料以上の安全性上の問題となる事象は認められなかったと評価した (2011175703) 。 研究2: 長期継続摂取試験 対象:BMIが25 kg/m2以上30 kg/m2未満でかつ、腹部の内臓脂肪面積 (VFA) が80cm2以上170cm2未満の成人男女109名。 方法:本試験は、二重盲検無作為化並行群間比較試験法で実施した。試験期間としては、事前観察期間を4週間、試験飲料摂取期間を12週間、事後観察期間を4週間設けた。事前観察期間の開始時の測定値を用い、最小化法で被験者を2群 (クロロゲン酸飲料摂取群、プラセボ摂取群) に分けた。試験飲料摂取期間中、被験者はクロロゲン酸飲料またはプラセボ飲料のいずれかを1日1本摂取した。クロロゲン酸飲料はクロロゲン酸類297 mg含み、プラセボ飲料は、クロロゲン酸類を低減したコーヒー飲料とした。解析対象は、事前観察期間中に腹部脂肪面積の変化が少なかった者109名 (クロロゲン酸飲料摂取群53名、プラセボ摂取群56名) とした。安全性の面において、血液検査、尿検査、および問診の結果を評価した。検査は、試験飲料の摂取開始時を0週目として、-4週目、0週目、4週目、8週目、12週目、および16週目に実施した。 結果:血液検査項目において、クロールやカリウムなどで群間差が認められたが、他の血液検査項目も含め、臨床上問題となる大きな値の変化は認められなかった。尿検査項目で有意な変動は認められなかった。有害事象において、風邪や疲労に起因する一過性の頭痛や試験前からの足の痛みが報告されたが、いずれも自然回復し、試験責任医師によって試験飲料との関連性は無いと報告された (2009211385) 。
(2011175703) 薬理と治療. 2010 38(9); 825-832. (2009211385) 薬理と治療. 2009: 37(4); 333-344.
ヘルシアコーヒー微糖ミルクの関与成分クロロゲン酸類について、変異原性試験、単回投与毒性試験、反復投与毒性試験および催奇形性試験を行った結果、いずれの試験においても毒性は認められなかった (1) 。
(1) 社内報告書
研究1: 12週間継続摂取有効性試験 対象BMIが25 kg/m2以上30 kg/ m2未満でかつ、腹部の内臓脂肪面積 (VFA) が80 cm2以上170 cm2未満の成人男女109名。 方法:本試験は、多施設無作為化二重盲検プラセボ対照並行群間比較試験法で実施した。試験は事前観察期間を4週間、試験飲料摂取期間を12週間、事後観察期間を4週間設けた。事前観察期間の開始時の測定後に、ランダムに被験者を2群 (クロロゲン酸飲料摂取群、プラセボ摂取群) に分けた。試験飲料摂取期間中、被験者はクロロゲン酸飲料またはプラセボ飲料のいずれかを1日1本摂取した。クロロゲン酸飲料はクロロゲン酸類297 mg含み、プラセボ飲料は、クロロゲン酸類を低減したコーヒー飲料とした。解析対象は、事前観察期間中に腹部脂肪面積の変化が少なかった者109名 (Per Protocol Set;PPS クロロゲン酸飲料摂取群53名、プラセボ摂取群56名) とした。検査項目は、腹部脂肪面積 (内臓脂肪面積、皮下脂肪面積 (SFA) 、全脂肪面積 (TFA)) 、理学検査項目として身長、体重、体脂肪率、ウエスト周囲長、ヒップ周囲長、血圧 (収縮期血圧、拡張期血圧) 、その他項目として、血液学検査、血液生化学検査、尿検査、および問診とした。検査は、試験飲料の摂取開始時を0週目として、-4週目、0週目、4週目、8週目、12週目、および16週目に実施した。 結果:〔腹部脂肪面積〕被験者109名 (PPS、クロロゲン酸飲料摂取群53名、プラセボ摂取群56名) について解析を行った。12wk時の0wkに対する変化量 (Δ12wk) に関して、クロロゲン酸飲料摂取群では-4.4 cm2、プラセボ摂取群では3.6 cm2となり、クロロゲン酸飲料摂取によるVFAの低減効果が認められた。またSFA、TFAに関してもクロロゲン酸飲料摂取群においてプラセボ摂取群と比較して減少が認められた。 〔理学検査項目〕体重、BMI、ウエスト周囲長、およびヒップ周囲長において、プラセボ摂取群と比較してクロロゲン酸摂取群に低減効果が認められた (2009211385) 。 研究2: 1週間継続摂取クロスオーバー試験 対象:健常成人男性7名 (クロスオーバー試験) 。 方法:本試験は、7名の健常成人男性を用い、二重盲検クロスオーバー試験法で実施した。被験品は、クロロゲン酸飲料およびプラセボ飲料とした。試験期間中は、被験品以外のコーヒーを含む食品および茶類の摂取を禁止とした。試験スケジュールは、初めの1週間をウォッシュアウト期間とし、次に被験品摂取第1期間として7日間、クロロゲン酸飲料またはプラセボ飲料を1日1本摂取させ、1日目および8日目に試験日を設けた。その後、再度ウォッシュアウト期間 (1週間) を設け、飲料の種類を変えて同様の試験を行いクロスオーバー試験とした。 試験日の前日の夕食後、少なくとも12時間は絶食とし、以降は水のみ飲用可とした。試験日の呼気分析は、安静時呼気の測定後、被験品 (試験飲料またはプラセボ) および指定食摂取後、30分後に安静時呼気を測定し、以降210分まで30分間隔で測定した。 結果:〔酸素消費量 (エネルギー消費量)〕試験開始時の安静時における酸素消費量の経時変化において、両群間の酸素消費量に差は認められなかった。一方、摂取1週間後では、プラセボ群に対し試験飲料群において、食事摂取30および60分後の酸素消費量が高値を示した。また、摂取1週間後における酸素消費量の平均値は、食事摂取60、90、120、150分後において増加を認めた。 〔呼吸商、脂肪燃焼量〕摂取1週間後において、呼吸商に差は認められなかったが、脂肪燃焼量の経時変化は、食事摂取90分後で試験飲料群はプラセボ群に対して高値を示し、脂肪燃焼量の増加が認められた。また、摂取1週間後における脂肪燃焼量の平均値は、食事摂取90、120分後において、試験飲料群はプラセボ群に対して高い値を示し、特に食後早期の脂肪燃焼増加が認められた (2011149729) 。
(2009211385) 薬理と治療. 200937(4);333-344. (2011149729) J Health Sci. 2010:56(6);745-751.
研究1: 対象C57BL/6Jマウス (食餌依存性肥満モデルマウス、6週齢、雄性) 、10匹×4群。 方法:摂取させる食餌によってマウスを4群に分け、低脂肪食群、対照群 (高脂肪・高蔗糖食) 、0.5%CPP群 (高脂肪・高蔗糖食にCPP (コーヒーポリフェノール) を0.5%添加した食餌) 、1%CPP群 (高脂肪・高蔗糖食にCPPを1%添加した食餌) とした。各群において15週間飼育した。飼育後に体重を測定し、対照群と0.5%CPP群および1%CPP群を比較した。 結果:対照群とCPP群で食餌の摂食量に差はなかった。対照群は食餌依存性の肥満を示したが、1%CPP群において体重増加の抑制が認められた (PMID:20943752) 。 研究2: 対象:C57BL/6Jマウス (食餌依存性肥満モデルマウス、6週齢、雄性) 、10匹×4群。 方法:摂取させる食餌によってマウスを4群に分け、低脂肪食群、対照群 (高脂肪・高蔗糖食) 、0.5%CPP群 (高脂肪・高蔗糖食にCPP (コーヒーポリフェノール) を0.5%添加した食餌) 、1%CPP群 (高脂肪・高蔗糖食にCPPを1%添加した食餌) とし、各群において15週間飼育した。15週目に解剖を行い、内臓脂肪である白色脂肪組織を採取して、内臓脂肪組織重量 (腎周囲脂肪、後腹膜脂肪、副睾丸周囲脂肪、腸管膜脂肪) を測定した。副睾丸周囲の白色脂肪組織から抽出したRNAをRT-PCRにより遺伝子発現解析を行い、脂肪細胞の肥大化 (マクロファージ浸潤) の程度を評価した。 結果:対照群と比較して、1%CPP群において内臓脂肪組織重量の増加抑制が認められた。また、副睾丸周囲脂肪では、低脂肪食群に対して対照群で肥大化が観察され、1%CPP群において脂肪細胞の肥大化を示すF4/80、CD68、MCP-1の増加抑制が認められた (PMID:20943752) 。 研究3: 対象:C57BL/6Jマウス (食餌依存性肥満モデルマウス、6週齢、雄性) 、10匹×4群。 方法:摂取させる食餌によってマウスを4群に分け、低脂肪食群、対照群 (高脂肪・高蔗糖食) 、0.5%CPP群 (高脂肪・高蔗糖食にCPP (コーヒーポリフェノール) を0.5%添加した食餌) 、1%CPP群 (高脂肪・高蔗糖食にCPPを1%添加した食餌) とし、各群において15週間飼育した。15週目に解剖を行い、肝臓を採取して重量の測定を行った。さらに肝臓の一部を用いて凍結切片を作製し、オイル赤O染色液で染色した。さらにFolchらの方法に従い、肝臓より脂質を抽出して肝臓脂質の定量を行い肝臓への脂肪蓄積抑制作用を評価した。 結果:肝臓をオイル赤Oで染色した結果、対照群では肝臓が広範囲に赤く染色されたが、1%CPP群ではほとんど染色されず、また、肝臓中の中性脂肪と総コレステロールを定量した結果、両者とも対照群で顕著に増加したが、CPP群では、中性脂肪は1%CPP群で、総コレステロールは用量依存的に抑制されていたことから、肝臓への脂肪蓄積抑制作用が認められた (PMID:20943752) 。
(PMID20943752) Am J Physiol Endocrinol Metab. 2011:300(1);E122-133.
